本文刊載于《集成技術》2022年第3期“新能源新材料專欄”
司韶康1,2 張 蕾 1,3* 溫佳鑫3 于淑會1 曹秀華4 付振曉4 孫 蓉 1
1 中國科學院深圳先進技術研究院 深圳先進電子材料國際創新研究院 深圳
2 中國科學技術大學納米科學技術學院 蘇州
3 南方科技大學前沿與交叉科學研究院 深圳
4 廣東風華高新科技股份有限公司先進材料和電子元器件國家重點實驗室 肇慶
引用格式: 司韶康, 張蕾, 溫佳鑫, 等. 高四方性超細 BaTiO3 納米粉體的制備與性能研究 [J]. 集成技術, 2022, 11(3): 108-120.
Si SK, Zhang L, Wen JX, et al. Fabrication and properties of ultra-fine BaTiO3 particles with high tetragonality [J]. Journal of Integration Technology, 2022, 11(3): 108-120.
摘要
高四方性的 BaTiO3 超細粉體是下一代多層陶瓷電容器的關鍵材料。該文探究了砂磨介質尺寸和原料 TiO2 晶相對反應物活性、產物介電性能的影響,并利用砂磨固相法成功合成了高四方性 BaTiO3 超細粉體。分析場發射掃描電子顯微鏡照片和 X 射線光電子能譜發現,細砂磨介質粉碎原料的效率更高,機械活化作用更強。Raman 光譜和 X 射線衍射圖譜顯示,在高能砂磨過程中,TiO2 由銳鈦礦相先后轉變為 TiO2-II 相、金紅石相。分析微商熱重曲線和 X 射線衍射,結果表明,砂磨介質更能有效降低反應溫度和抑制 Ba2TiO4 的生成。此外,高分辨透射電子顯微鏡圖像揭示了 BaTiO3 的形成是 Ba2+ 向 TiO2 晶格擴散的過程。該文相關實驗結果表明,利用直徑為 0.1mm 的 ZrO2 磨球對銳鈦礦相 TiO2 和 BaCO3 混合物砂磨 4 h,并在 1100 °C 煅燒 3 h 后,獲得了平均粒徑為 186 nm、四方性為 1.0092 且分散性良好的 BaTiO3 粉體,該粉體在1250 °C 燒結的陶瓷相對密度為 96.11%,居里點(137.8 °C)的介電常數峰值為 8 677。
1 引 言
電子信息技術的突飛猛進,加快了電子元器件升級換代的速度。高性能電子陶瓷材料及無源電子元件是電子產品重要的實體,在信息產業中的地位不亞于鋼鐵在傳統工業中的地位,其發展具有重要的戰略意義。片式多層陶瓷電容器(Multi-layers Ceramic Capacitors,MLCCs)是一種新型、微型化、片式化的高精度電容器,是片式容阻感元件中用量最大、發展最迅速的核心元件[1-2]。近年來,隨著電子設備及其元器件的小型化、高可靠性、薄型化和低成本化,介質材料的晶粒尺寸不斷向納米級別發展。對 MLCCs 而言,實現高容量、小型化、薄層化和高可靠性等性能要求的基礎是減小基料鈦酸鋇(BaTiO3,BT)的粒徑尺寸,即粉體超細化。為實現MLCCs的這些性能需求,基料 BT 的晶粒尺寸需要控制在 200 nm 以下。目前,超細 BT 的合成方法包括水熱法[3-5]、固相法[6-9]、溶膠- 凝膠法[10-12]、熔鹽法[13 - 17]等。其中,水熱法和固相法是工業中常用的兩種工藝。但是,水熱法合成 BT 的步驟復雜、成本高、廢液處理復雜,產品易存在羥基缺陷,且該方法的合成條件控制苛刻,技術壁壘高。固相法則以其成本低、工藝簡單、合成的 BT 粉體缺陷少[18-20]、結晶度高的優勢成為工業中最常用的工藝,但傳統固相法由于較高的煅燒溫度(>1000 °C)常導致 BT 粉體的粗晶化和團聚化。使用超細的原料粉體雖然可以降低煅燒溫度[21-25],避免粗晶化和團聚化,但同時帶來了成本增加的問題,因此,工業上急需一種經濟實用的生產超細原料粉體的手段。有研究發現,砂磨工藝是一種獲得超細粉體的有效方法[26-28]。本文采用砂磨工藝,通過研究不同直徑(0.1 mm 和 0.3 mm)的 ZrO2 砂磨介質和不同晶型 TiO2(銳鈦礦相和金紅石相)對煅燒溫度及 BT 性能的影響,確定了砂磨固相合成超細 BT 粉體的最優工藝,同時對其反應機理進行了探究。
2 實驗方法
2.1 樣品制備
本研究中使用的原料為BaCO3 (比表面積 1.37 m2/g,純度99.8%,阿拉丁試劑(上海)有限公司)、銳鈦礦相TiO2(比表面積8.7m2/g,純度 99.0%,阿拉丁試劑(上海)有限公司)和金紅石相 TiO2(比表面積 10.9 m2/g,純度 99.0%,上海麥克林生化科技有限公司)。以去離子水為溶劑,按照等摩爾比將 BaCO3 、TiO2 混合攪拌均勻后進行砂磨。砂磨介質為ZrO2 球,直徑分別為 0.1 mm 和 0.3 mm。將利用砂磨機(型號 NT-V1,東莞市瑯菱機械有限公司)高速砂磨 4 h 后的漿料進行干燥處理,得到的混合粉體記作樣品 S1、S2、S3 和 S4。其中,S1、S2 使用的是直徑為 0.3 mm 的 ZrO2 磨球,S3、S4 使用的是直徑為 0.1 mm 的 ZrO2 磨球;S1、S3 使用的是銳鈦礦相TiO2,S2、S4 使用的是金紅石相TiO2,具體配料見表 1。將 S1、S2、S3 和 S4 于 1100 °C 煅燒 3 h 后,加入一定量的聚乙烯醇(Polyvinyl Alcohol,PVA )并壓制成圓片形生坯(直徑為 5 mm,厚度為 2 mm),生坯在空氣氣氛中分別于 1250 °C、1300 °C、1350 °C 燒結 2 h 后可得到純相 BT 陶瓷片,用于測試介電性能。
2.2 樣品表征
原料粉體的比表面積通過比表面積及微孔分析儀(型號 ASAP2020,麥克默瑞提克(上海)儀器有限公司)進行測量。粉體及陶瓷的形貌使用場發射掃描電子顯微鏡(型號 NOVA NANOSEM 450 ,賽默飛世爾科技有限公司,美國)觀察,并利用 ImageJ 軟件對形貌照片進行統計,從而得到粉體顆粒的平均粒徑和陶瓷平均晶粒尺寸(DA.V.)。樣品價電子結合能使用 X 射線光電子能譜(型號 ESCALAB 250Xi,賽默飛世爾科技有限公司,美國)進行表征。TiO2砂磨前后的相轉變通過室溫 Raman 光譜(型號 LabRAM HR Evolution,堀場儀器(上海)有限公司)進行表征,測試時使用的激光光源波長為 532 nm。粉體的晶體結構通過 X 射線衍射儀(型號 Smartlab SE,日本理學株式會社,日本)確定,使用 JADE 軟件計算 BaTiO3 的晶格參數(a 和 c)。使用熱重分析儀(型號 Q-600,梅特勒-托利多集團,瑞士)在 100 mL/min 高純干空氣吹掃下,將砂磨后的樣品以 10 °C/min 的速度從 25 °C升至 1 250 °C,記錄升溫過程中的重量變化。樣品的微觀結構采用高分辨場發射透射電子顯微鏡(型號 FEI-Talos F200X,賽默飛世爾科技有限公司,美國)進行表征。陶瓷的密度利用阿基米德排水法進行計算。介電性能使用阻抗分析儀(型號 Agilent E4980A,安捷倫科技有限公司,美國)進行測試,以 3 °C/min 的速度從室溫升至 200 °C,使用頻率為 1 kHz 的 1V 交流電壓測試其電容,然后根據平板電容模型換算出介電常數。
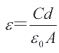
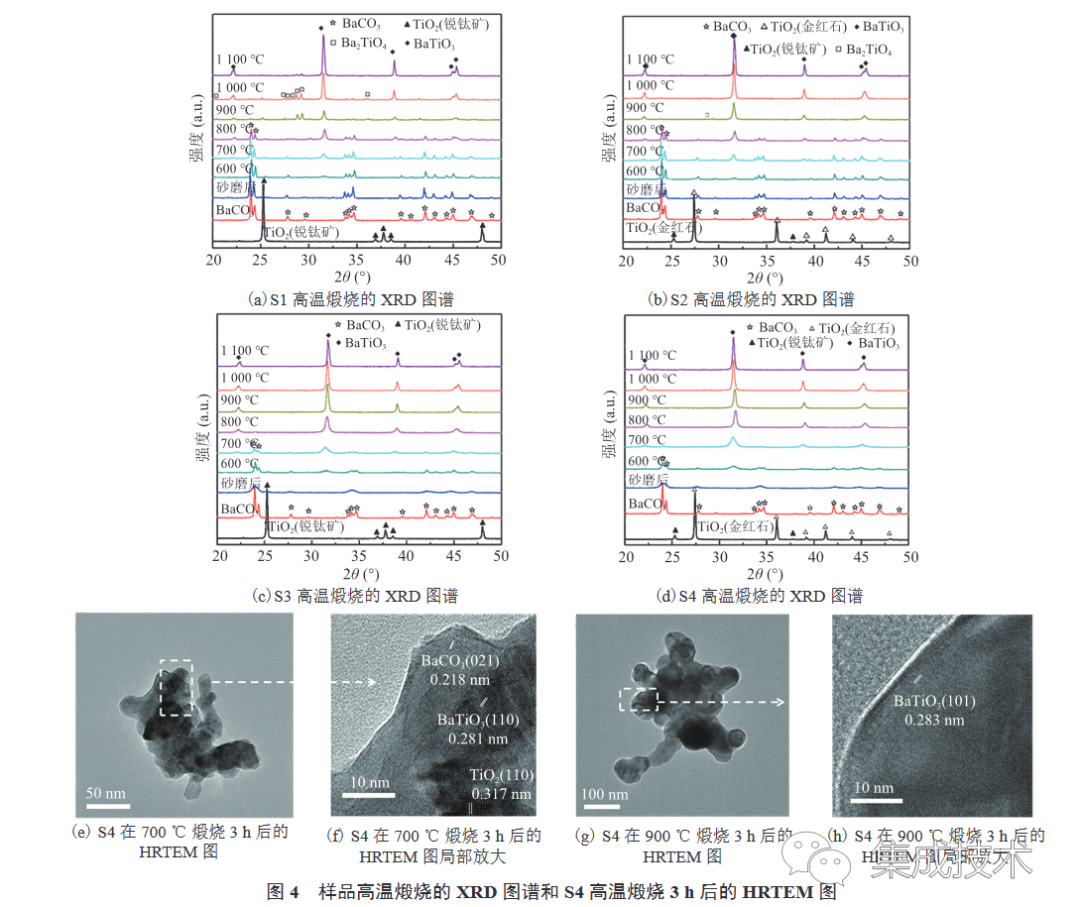
其中,d 為陶瓷片的厚度;C 為電容;ε0為真空介電常數;A 為陶瓷片的橫截面積。
3 結果與討論
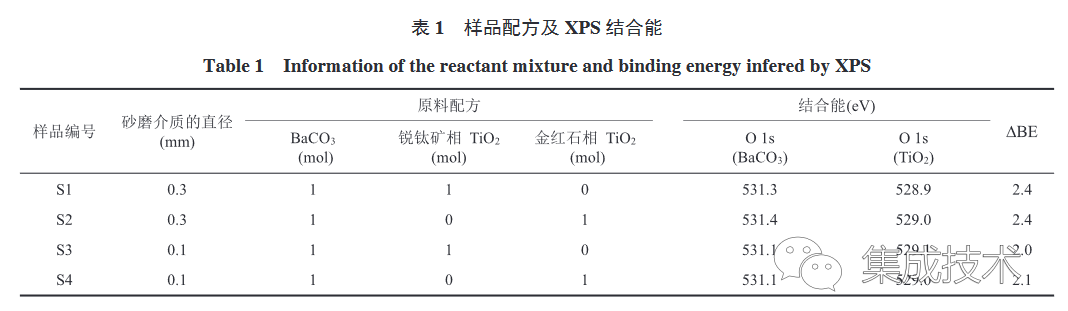
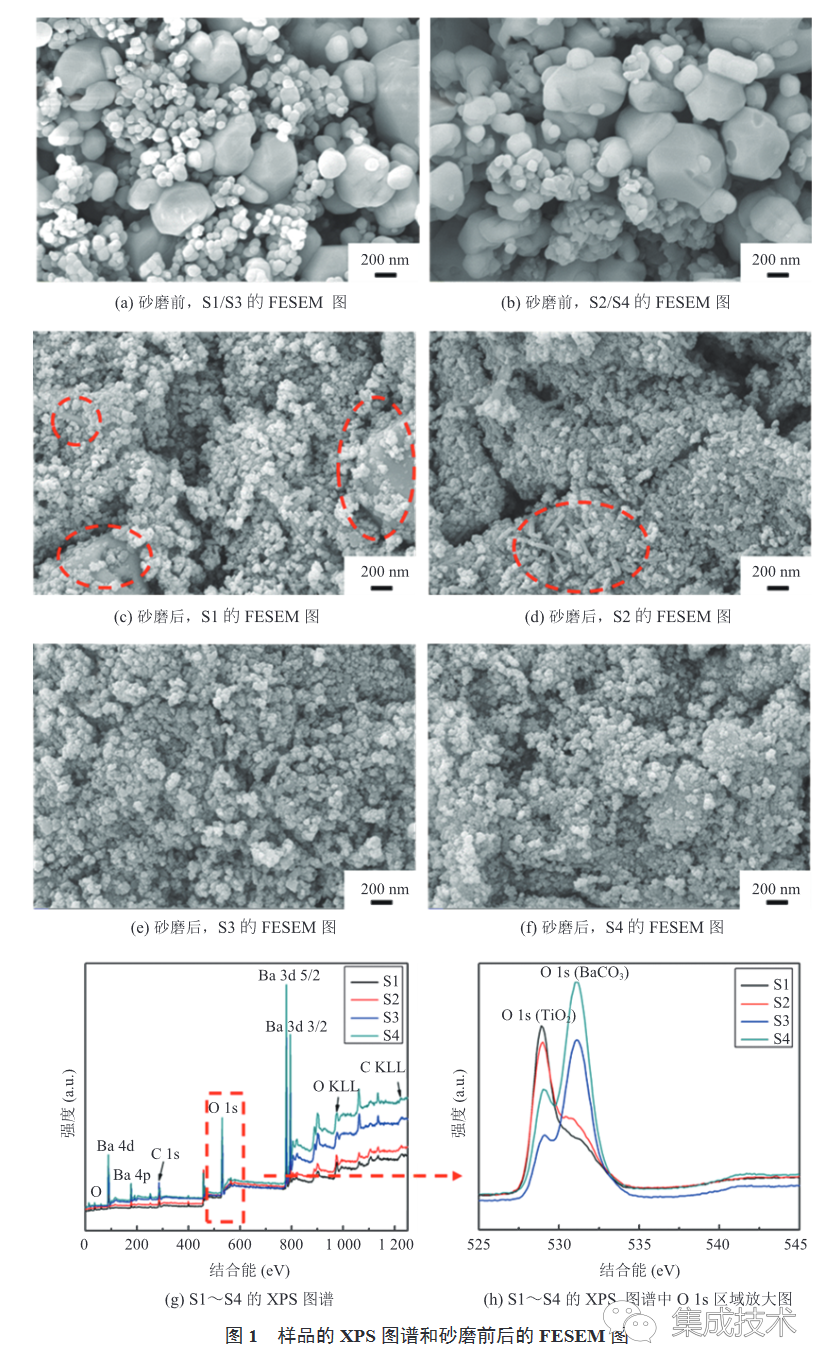
1(a)~(f)為 TiO2與 BaCO3 混合物砂磨前后的場發射掃描電子顯微鏡(Field Emission Scanning Electron Microscope,FESEM)圖像。由圖可知,砂磨前混合物顆粒尺寸相差較大,小顆粒團聚明顯;砂磨 4 h 后,混合物的粒徑顯著減小,相對均勻。與 S3、S4 相比,S1 和 S2 的粒徑尺寸更大、團聚更多,且有棒狀顆粒。這可能是由于較大直徑(0.3 mm)的ZrO2 砂磨介質在砂磨過程中提供的剪切和碰撞頻率較小,導致其對混合物的砂磨效果較差。為了進一步分析砂磨介質對樣品砂磨效果的影響,對樣品 S1~S4 的 X 射線光電子能譜(X-ray Photoelectron Spectroscopy,XPS)進行測試,測試結果如圖 1(g)~(h)所示。圖 1(h)中兩個 O 1s 峰位對應的結合能標志著TiO2 中 Ti—O 鍵和 BaCO3 中 Ba—O 鍵的結合強度[29]。由圖 1(h)可知,S3 和 S4 中 O 1s(BaCO3)的相對強度較 S1 和 S2 有了明顯提升,由于 XPS 的穿透深度有限,僅能測量物質表面層,所以 S3 和 S4 中 BaCO3 的信號更強意味著 S3 和 S4 中BaCO3 暴露的表面積更多,這表明與 S1 和 S2 相比,S3 和 S4 的 BaCO3 細化程度更高。由表 1 可得,S3 和 S4 的 O 1s 結合能差值(ΔBE)小于 S1 和 S2,說明 S3 和 S4 中 O 原子的化學狀態更接近,反應物活化性能更高。因此,較小尺寸砂磨介質的機械活化作用更強。
為了驗證砂磨帶來的機械活化作用對TiO2晶型轉變的影響,本實驗以去離子水為分散介質,利用直徑為 0.1 mm 的ZrO2 砂磨介質對銳鈦礦相 TiO2 和金紅石相 TiO2砂磨 4 h,TiO2砂磨前后的室溫 Raman 光譜如圖 2(a)~(b)所示。
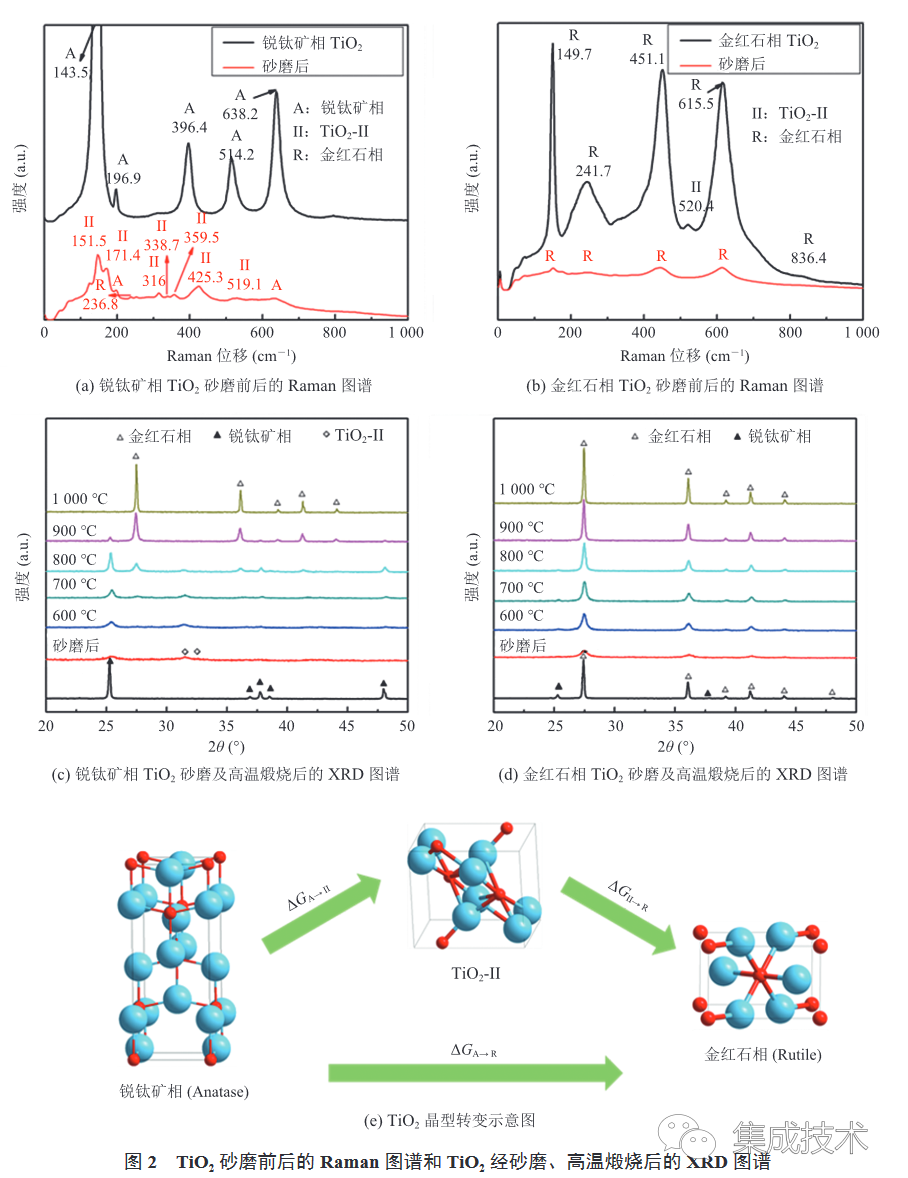
圖 2(a)為銳鈦礦相TiO2砂磨前后的 Raman 圖譜,由圖可知,TiO2砂磨前呈現出典型的銳鈦礦相特征峰[30],分別為 143.5 cm-1(Eg)、196.9 cm-1(Eg)、396.4cm-1 (B1g)、514 . 2cm-1 (A1g+B1g)、638.2cm-1(Eg);砂磨后則增加了TiO2-II 相(TiO2的一種高壓穩定相,結構同-PbO2,屬于正交晶系,Pbcn 空間群,鈮鐵礦型結構)特征峰[31],分別為 151.5 cm-1(B3g)、171.4cm-1(Ag)、316 cm-1(B1g)、338.7 cm-1(B2g)、359.5 cm-1(B2g)、425.3 cm-1(Ag)、519.1 cm-1(B2g),此外,還增加了金紅石相TiO2的特征峰:236.8cm-1(Eg)[32],即砂磨后的 Raman 圖譜呈現出銳鈦礦相、TiO2-II 、金紅石相三相共存的現象。這一結果與 Ashiri 組[33]報道的銳鈦礦相TiO2經 10 h 砂磨后,將完全轉變為金紅石相的結論不一致。原因可能是本實驗的砂磨時間較短,不足以使TiO2 由銳鈦礦相完全轉變成金紅石相,從而得到了TiO2 的三相混合物。圖 2(b)為金紅石相 TiO2砂磨前后的 Raman 圖譜,由圖可知,TiO2 砂磨前呈現出典型的金紅石相及 TiO2-II 相特征峰,砂磨后則完全呈現出金紅石相特征峰。進一步對不同晶型TiO2砂磨后的產物進行了高溫煅燒,煅燒產物的 X 射線衍射(X-ray Diffraction,XRD)圖譜如圖 2(c)~(d)所示。從 600 °C 升至 1000 °C 過程中,TiO2(銳鈦礦相)砂磨后的產物由于同時包含銳鈦礦相、TiO2-II 相和金紅石相,需要吸收較多能量進行相轉變,故當溫度達到 1000 °C時,TiO2(銳鈦礦相)才完全轉變為TiO2(金紅石相)。此外,兩種不同相的 TiO2經過砂磨后,衍射峰變寬,峰強降低,這是由于砂磨給物料輸入了巨大能量,使得原料晶格發生畸變,因此衍射峰變寬,同時晶格焓降低,反應活性升高,從而降低了 BaCO3 與TiO2的固相反應溫度[34]。通過以上實驗結果可知,本研究中銳鈦礦相TiO2經過短時間砂磨或是高溫煅燒都會產生銳鈦礦相(Anatase)→TiO2-II 相→金紅石相(Rutile)的相轉變(如圖 2(e)所示)。這一相變順序是由于 TiO2-II 相、金紅石相、銳鈦礦相之間的相變吉布斯自由能大小滿足 ΔGA→II<ΔGII→R<ΔGA→R[35]。
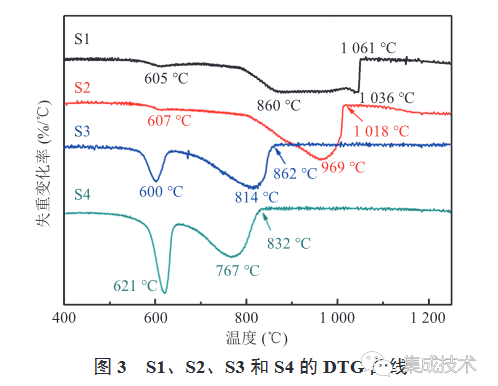
為了明確合成 BaTiO3 的反應溫度,對樣品 S1~S4 進行了熱重分析。圖 3 熱重分析的 DTG 曲線中,600~621 °C 的第一個失重峰對應的是 BaCO3 與TiO2 一步生成 BaTiO3 的過程,即反應(1);760~860°C 的失重峰對應的是 BaCO3 分解后與TiO2 形成 BaTiO3 的過程,即反應(2)、(3)。通過對圖 3 中 S1~S4 的 DTG 曲線綜合分析可知,隨著砂磨介質 ZrO2尺寸的減小,第二個失重峰的位置逐漸向低溫區偏移,這表明較小尺寸的砂磨介質更利于降低 BaCO3 與TiO2 的固相反應溫度。同時,S4 的第一個失重峰強度比 S3 的更大,說明 S4 中反應(1)的占比更多。S4 中反應(1)進行得更充分可能是因為 S4 粒子的表面能更高。S3 吸收的砂磨能量中有一部分用于TiO2 從銳鈦礦相轉變為金紅石相,S4 吸收的砂磨能量則全部轉化成表面能,因此,S4 粒子的表面能更高,更容易在低溫段反應。此外,圖 3 中 S1 除了 860 °C 的峰,還有一個 1036 °C 的峰——BaCO3 的熱解峰,由于 S1 混料不夠充分,少量 BaCO3 接觸不到 TiO2,固相反應后處于被 BaTiO3 包夾、隔離空氣的狀態,這一狀態下熱分解的溫度有較大提升,高達 1000 °C。
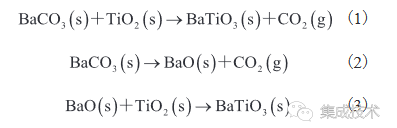
根據圖 3 的 DTG 曲線,將樣品在 600~1 100 °C中分別煅燒 3 h,煅燒產物的 XRD 圖譜如圖 4(a)~(d)所示。由圖 4(a)~(d)可知,當煅燒溫度為 600 °C 時,產物中含有 BaCO3、TiO2 和 BaTiO3 3 種相。其中,S3 和 S4 的 BaCO3 相衍射峰比 S1 和 S2 的要弱,表明 S3 和 S4 中 BaCO3 的轉化率較高,這與圖 3 中 S3 和 S4 在 600 °C、621 °C 的第一個失重峰面積比 S1、S2 大相印證。當煅燒溫度升至 900 °C 時,S1 和 S2 開始生成 BaTiO3 純相,但仍存在少量 Ba2TiO4 相;而煅燒溫度升至 800 °C 時,S3 和 S4 中 BaCO3 和 TiO2相衍射峰已消失,僅存 BaTiO3 相。據 Fujikawa 等[36]的研究結果可知,當 BaCO3 過量,且煅燒溫度高于 850 °C 時,會得到副產物 Ba2TiO4。而本研究中,較粗的砂磨介質使 S1 和 S2 混合的均勻性較差,導致 BaCO3 局部過量產生Ba2TiO4 。因此,使用較細的砂磨介質可有效降低固相反應溫度防止Ba2TiO4副產物的生成。該結論與 Buscaglia 等[37]和 Yanagawa 等[29]的研究結果一致。
為了深入探究 BaTiO3 的形成機理,根據 XRD 圖譜,本實驗對 S4 在 700 °C 和 900 °C 煅燒合成 BaTiO3的產物用高分辨透射電子顯微鏡(High Resolution Transmission Eectron Microscopy,HRTEM)進行觀察和分析。
由圖 4 (e)~(f)可知,當煅燒溫度為 700 °C 時,S4 呈現出 TiO2/BaTiO3/BaCO3 的三層結構;當煅燒溫度升至 900 °C 時,S4 則呈現出BaTiO3 的晶格結構。這一結果與 XRD 圖譜相互印證,同時進一步證明了 BaCO3 與TiO2反應合成 BaTiO3 的過程,是 Ba2+、O2- 向 TiO2 晶格擴散的過程[38]。本研究中利用砂磨工藝減小了 BaCO3 與TiO2原料的粒徑,極大地增加了二者的反應面積,縮短了 Ba2+→TiO2擴散的路徑,有效抑制了副產物 Ba2TiO4 的形成,同時降低了BaTiO3的合成溫度。
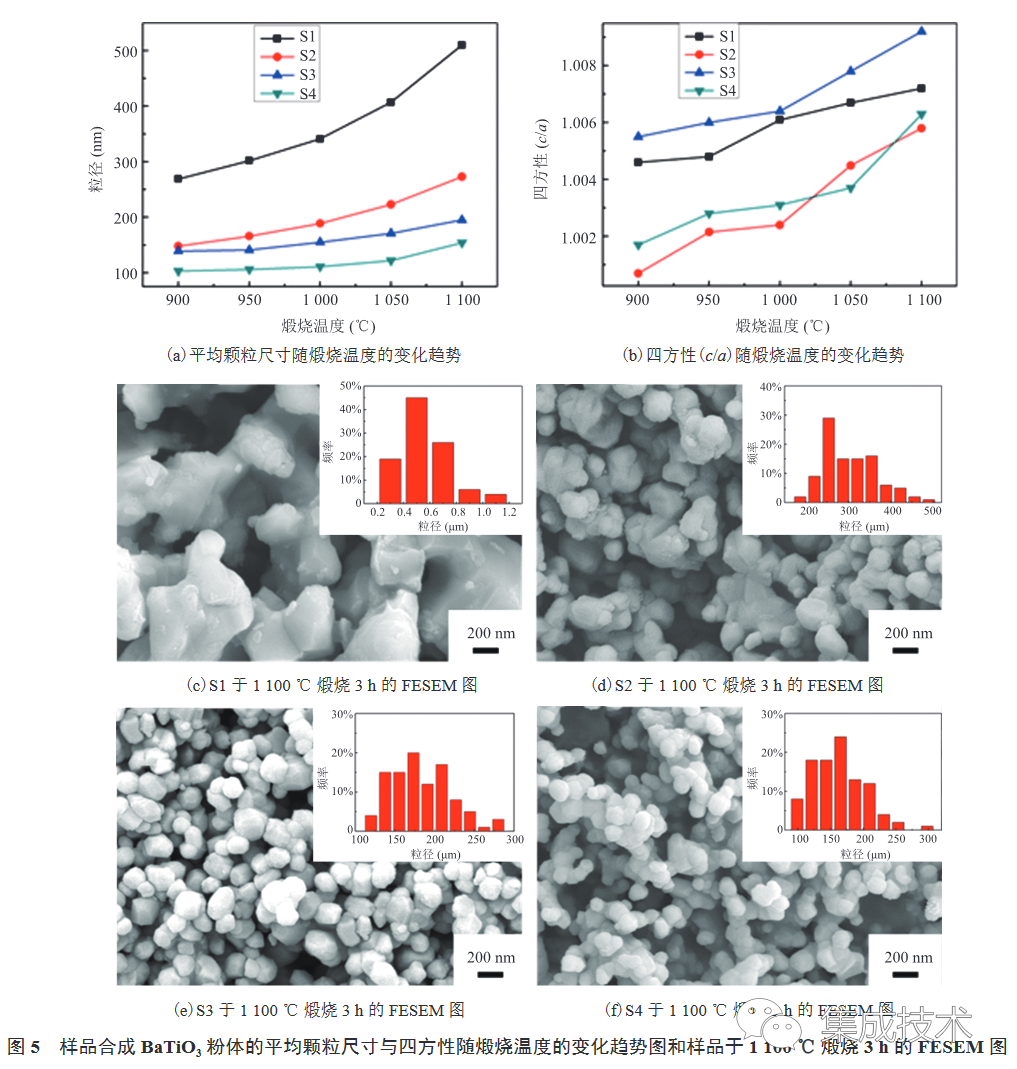
圖 5(a)~(b)為 S1~S4 合成的BaTiO3 粉體平均顆粒尺寸和四方性(c/a)隨煅燒溫度(900~1 100 °C)的變化圖。由圖可知,BaTiO3的平均顆粒尺寸和四方性均會隨著煅燒溫度的升高而增大。一般來說,BaTiO3 的四方性與顆粒尺寸呈正相關[39]。但在本研究中,當煅燒溫度相同時,S1 和 S2 的平均顆粒尺寸大于 S3 和 S4,且 S4 的平均顆粒尺寸最小;但 S3 和 S1 的四方性大于 S4 和 S2,且 S2 的四方性最小。可能是因為與金紅石相TiO2相比,S1 和 S3 使用的銳鈦礦相的晶胞密度較低,離子排列較為疏松,晶格間隙大,有利于 Ba2+ 擴散至TiO2 中,從而提高其四方性;而 S2 和 S4 中的金紅石相TiO2的結構緊密,且最為穩定,不利于 Ba2+ 擴散至TiO2 中,從而導致四方性小。圖 5(c)~(f)為 S1~S4 在煅燒溫度為 1100 °C 時合成BaTiO3 粉體的 FESEM 圖。由圖可知,在相同煅燒溫度下,S1 合成的 BaTiO3 粉體粒徑最大,而 S3 和 S4 合成的 BaTiO3粉體粒徑較小。
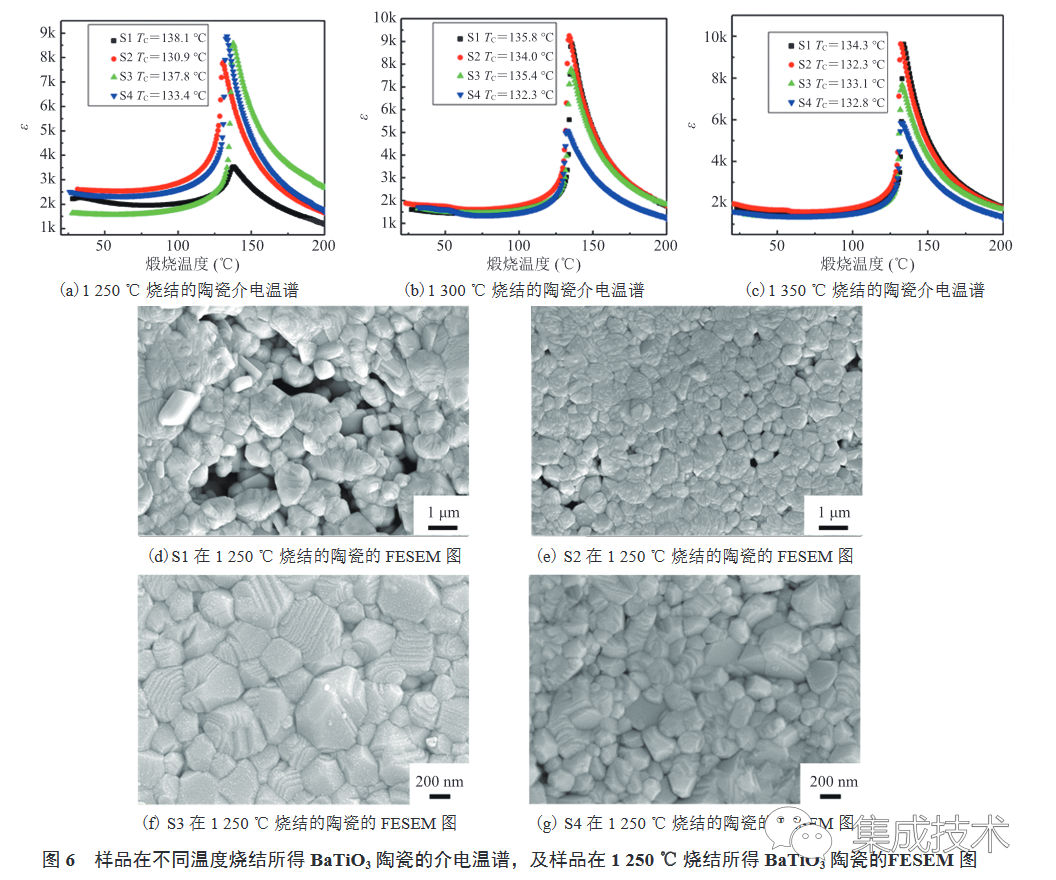
圖 6(a)~(c)為樣品在不同燒結溫度下得到的 BaTiO3 陶瓷的介電溫譜。由圖 6(a)~(c)可知,S1~S4 都呈現出 BaTiO3 明顯的相變峰,該峰表示 BaTiO3 陶瓷四方相→立方相的轉化,其溫度稱為居里點(TC)。
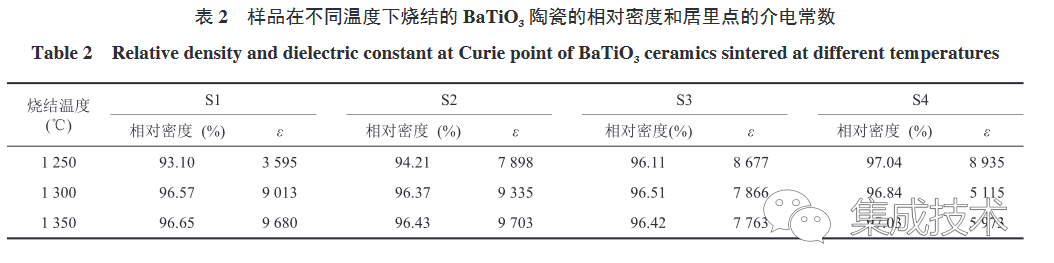
樣品的相對密度和居里點所對應的介電常數如表 2 所示,隨著燒結溫度的升高,S1 和 S2 合成的 BaTiO3 陶瓷的相對密度和介電常數增大,而 S3 和 S4 的相對密度和介電常數基本保持不變,甚至還有部分減小。這是由于 S3 和 S4 的粉體粒徑較小,燒結活性較高,在較低的溫度(1250 °C)下即可燒結致密;而 S1 和 S2 的粒徑較大,燒結活性較低,在較高的溫度(>1300 °C)下才能燒結致密。當燒結溫度為 1250 °C 時(圖 6(a)),介電常數峰值滿足關系:
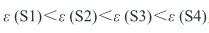
這與 Wang 等[40]提出的原始粉體顆粒的尺寸越大,燒結后介電常數越高的觀點相悖。對比不同樣品在 1250 °C 燒結后的 FESEM 圖(圖 6(d)~(g)),發現粉體顆粒尺寸大的 S1 和 S2 峰值低的原因是其低密度及高氣孔率劣化了介電常數[41-42]。隨著燒結溫度的升高,S1 和 S2 逐漸致密,氣孔率減少,介電常數峰值也顯著升高,且高于 S3 與 S4。而 S3 與 S4 隨著燒結溫度升高,其密度基本不變但其介電峰值逐漸降低,這是由于晶粒增大而產生的更大應變,壓低了介電峰[38]。
4 結 論
本文明確了利用砂磨工藝合成高四方性 BaTiO3超細粉體的最優參數,并闡明了砂磨固相合成高性能 BT 粉體的原理。通過相關性能測試,結果顯示:直徑較小的 ZrO2 砂磨介質細化 BaCO3 與TiO2 粒徑的效率更高,能有效降低BaTiO3 BaTi 的煅燒溫度,并抑制副產物 Ba2TiO4 的生成。在砂磨過程中,TiO2會發生銳鈦礦相→TiO2-II 相→金紅石相的轉變。利用直徑為0.1 mm 的 ZrO2 砂磨介質,采用較粗粒徑的 TiO2(銳鈦礦)和 BaCO3 在 1100 °C 煅燒 3 h,可得到平均粒徑為 186 nm、四方性為 1.0092 的超細 BT 粉體,將該 BT 粉體于 1250 °C 燒結的陶瓷相對密度為 96.11%,居里點(137.8 °C)的介電常數峰值為 8 677。
//參考文獻
(掃描下方二維碼查看全文以及參考文獻)





